逆渗透设计浅谈
浏览次数:111次发表时间:2017-07-20
RO系统流程的要求很低:一只泵、一支膜和各种连接管。但,在RO设计上,若需考虑RO膜的最长使用寿命,使应用上能符合经济效益,就需要将系统设计得更精密。
在设计RO系统的各种流程,都是为确保系统能满足应用的需要,并提供最优化的膜性能。通常,膜的生产厂商必需提供膜资料给系统组装厂,以下是膜生产厂也需考虑的基本概念。
一、一般设计条件的调查
在RO系统设计之前,先了解一此限制条件和需求是十分重要的。RO系统的纯水回收、纯水水与系统的维护,都依赖於水源的水质;水源情况影响预处理的要求及RO系统的设计,换句话说,也会影响系统应用的经济性。因此,了解水源的水质及它是如何影响RO膜的应用,将帮助我们成功地设计RO预处理和RO系统。
RO系统的设计,必须先确定确水制造的流量,使满足高峰时所需使用的量。换句话说,如果纯水储存槽足够满足在某一天的最高峰的使用量,即可设计出RO系统适合於日平均使用量的需求。
水质纯度及纯水回数率的要求,决定必需使用那一种膜和决定是否需要两段式RO流程来增加水纯度的设计。使用阴阳离子交换器於RO的下段,以进一步使RO水变得更纯。若RO膜的阻隔率低於97.5%或95%以下,将会导致到下段离子交换系统再生频率提高一倍。
一旦渗透流的最小值和渗透水质的最大值被确定後,另外的参数也能被确定出来。也许还有尺寸限制RO单元,尺寸的限制设计错误会导致在RO系统中增加不必要的维护,举例来说:
如果RO系统中有一个螺旋形外壳紧则墙或垂直墙面安装,则更换膜元人牛就需要移动整机架。对技工来说,能很容易地接仪器面板、泵和膜元件,将会使维护变得十分容易。
RO系统依据水源的杂质含量,以及水的可变性和可用性而设计。假如城市用水的水源来自井水或地表水,它们的流量是根据变化无常的市政水情况而变的。在设计RO系统时,要想到各种最差的水源状况是很有必要的。
如果水压变化很大的话,说明市政或工厂用水分布系统设计不合理。可能进水管道或逆止阀尺寸不合理。(如果目前没有逆止阀,在安装RO前就须在市政管道安装逆止阀)。RO不能与建筑物的洒水系统同时使用同一水源。
水温也会极大的影响RO纯水流率,冬天的情况要考虑得多一点。某些机型热交换系统会用於加热RO进给水以增加出水,它通常需要更多的能量和操作费用,但也会减少RO系统中膜元件的使用量。在冷的月份中一个变速驱动器会加高压泵的输出(因水温过低造成)。
在使用生化剂对水源要加以分析,用於市政系统的典型的生化剂是自由氯或氯胺,因为这是一种可挥发性的化合物,意味着假如运送到远离现场的实验室中,它会散发到空气中,所以它的量必须在现场加以测量,测量工具能容易地从游泳池化学物供应商那里得到或者是从化工测试公司得到。用於市政用的水源,典型的自由氯的浓度是在0.3~0.8ppm之间。
氯胺的浓度要通过测试工具来分析其总含氯量。假如氯胺被用於市政的生物控制方面则必须加以注意,氯胺不如自由氯在杀死和抑制细菌方面有效,需要一些特殊的处理设备来除掉它。
水将被测试以确定细菌含量。如果有细菌存在并且生化剂浓度较低,在RO预处理中将持续地注入生化剂。在实验室中需要进行一种非常复杂的水源分析,这将用於决定水在RO系统中潜在水垢的形成,它会极大地影响RO纯水的回收率或对RO预处理要求。
二、特殊分析
(一)游泥密度指标(SDI):
1. 淤泥密度指标(SDI):
也称作污染指标,这个指标常用於水处理工业作为滤芯污染的指标,即是测量悬浮固体通过0.45μ过滤材的污染量,(图1)。
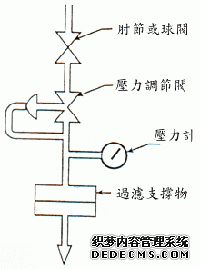
图1 测量淤泥密度指数(SDI)之装置
这种测量包括使水在正常压力下通过47毫米直径的过滤器,压力通为30PSI/m2。最初测量是500毫升的水通过过滤器所需的时间,然後在过滤器用15分钟後再测一次,这两次测量之间的比率用於决定过滤器污染的程度。
不幸的是,SDI测量不能在同一逆渗透元件上操作两次。在SDI测试时,所有的悬浮固体被从过 滤器中清除出来。对RO,一些比例不明的污染物会流过RO膜,最後留在RO废水中。因此,高SDI值并不代表RO膜已经很脏了。
SDI程序----
把SDI过滤设备靠近样品阀。
打开样品阀和设定压力为30psig,关闭样品阀并打过滤器外壳。
把47毫米,0.45微米的过滤器朝上,亮的一面朝着进给水处,在过滤器的外壳上安装一个支撑垫,把O型圈放进过滤器的顶部,弄湿过滤器关上外壳。
打开样品阀并迅速调整压力至30psig。
每隔5分钟,测量500毫升水注满量杯筒的时间,15分钟的测量将被用於计算SDI,除非过滤器插入少於15分钟。如果在这种情况下,计算10坌钟的测量值,若10分钟还不行的话,测量5分钟的测量值。
淤泥密度指标=100x(1-to/tT)/T在这里T是在第二次测量之前的时间(5、10或15分钟),to是最初的500毫升的时间,tT是在T分钟之後注满500毫升的时间。
典型的SDI值:
小於3 低的膜污染率
3-5 正常的污染率
大於5 高的污染率
举例:
运行5分钟测试因为有过多的污染在SDI过滤器中
最後注满量杯的时间:62秒
答案:SDI=100x(1-23/62)/5=12.6
对於如此高的SDI值,可能在RO膜元件中出现了明显的污染。必须采取措施以降低水中的污染物的浓度。一些预处理方法将在以後再讨论。
(二)浊度:
它是另一种用以指明RO膜中的污染度的测量方法,测量水样中的清澈程度。浊度计是用於测量由各种颗粒和悬浮固体所引起光的分布。
一旦浊度计的读数超过1.0,代表膜有被污染的倾向,这种读数是以浊度单位来表示的(NTU)或用一些有关的单位来表示。
与SDI测试一样浊度只是污染量的指标。高浊度并不一定意味着,高混浊的悬浮杂质都会沈积在RO膜上,反之亦然。事实上,一些膜污染会通过光线,而这些并不能在浊度测量上表示出来。
尽管不是最完善的分析工具,浊度计和SDI测试对测量RO进给水的特性还是有用的,它也能用於测量预处理设备除去RO膜中的污染的能力,所以我们建议这些测试应作为一种定期的基本测试以了解预处理介质过滤器的性能。
(三)Zeta电位:
有机悬浮固体群的壳表面一般带有负电荷,有了这一共同特性,各种简单的胶状团将互相排斥,它们不互相靠近而是相互排斥,所以不能形成一个大的胶状团,小的胶状团不像大的胶状团会克服水分子的力并保持悬浮。
当带有负电荷固体被逆渗系统浓缩後,会相互靠近。在这种情况下,固体就可能结合一起并形成一大团胶状体。大的胶状团会克服水的电荷和剪切力并保持悬浮状态,然後沉入溶液中并落到RO膜上。
Zeta电位是一种测量水中的悬浮颗粒总电荷的特性。一个负的Zeta电位表明水中含有自由负电荷特性的悬浮固体,这种固体更可能留在水中,一个中性的Zeta电位表明悬浮固体不会携带电荷去互相排斥,它们会形成一个大的胶状团并离开溶液。
Zeta电位测量常用於阳离子凝结剂注入系统的连接中。调整凝结剂浓度会得到介质过滤器中上流的中和的Zeta电位,悬浮固体更容易离开溶液被介质过滤器过滤出来,添加凝结剂不一定作为RO预处理的必备部份。
(四)流量测试器:
另一种用於凝结剂注射连接中的控制器,被称为流量测试仪(SCD)。这些设备使用一种机械活塞以产生一种高速水流,它会引起带电离子的运动并包围带有反向电荷悬浮颗粒(通常为负电荷)。它接着测量由移动电子所生产的电流,假如悬浮固体的电荷通过添加的凝结剂变成中性後,颗粒周围的自由电子将会减少,通过SCD将会产生一个较小的水流。
(五)水的化学性质:
知道基本水化学性质以了解RO系统中形成的水垢是十分重要的。当盐在水中溶解时,它能分离出阳离子(正电荷)和阴离子(负电荷)两部分,最常见的存在於水源中的离子如下表所示:
阳离子
镁离子Mg+2
阴离子
碳酸离子CO3-2
氯离子Cl-
硬度
钠离子Na+2
硷度
氢氧离子OH-
氟离子F-
钙离子Ca+2
钾离子K+
重碳酸离子HCO3-
硫酸根SO4-2
硝酸根NO3-
另外一些明显的离子也在下面表达出来:
阳离子
铝离子Al+3
铜离子Cu+2
矽酸根SiO2-
铁离子Fe+2或Fe+3
钡离子Ba+2
锌离子Zn+2
硫根S-
镁离子Mg+2
锶离子Sr+2
阴离子
磷酸根PO4-
RO进水的分析至少要测试第一组离子和pH值,但建议分析第二组离子(如果实验室条件允许的话)和浊度的测试。浓度是由每单位体积的水所含的杂质量算出的,一般用(mg/L)表示。因为水的密度是每升1克,大多数水溶液中1升水的重量为1000克,一千克水中1毫克相当於1百万克水中的一克,因此,这个比重我们称为每百万单位,在每升中所含有的毫克浓度就是典型稀释溶液中杂质的ppm表示。
实验室通常是用碳酸钙每升中的毫克数来表示,这是带电分子相对浓度的表示方法。它是由碳酸钙的分子重量和离子的价位相乘所得出的(分子重量为100和离子价位为2),可获得一个比例使原来重量浓度毫克/升转换为另外一个值,该值更能表达出溶液中带电离子的相对数量。假如一个离子的分子重量是碳酸钙的一半(转换参数是2),并且三价(即有三个电子价位)乘以钙或碳酸离子中的二价,它相对碳酸钙的浓度将会是基於离子重量的浓度的三倍(2x3÷2=3)。相对碳酸钙浓度的表达是十分有用的,因为它更好地表达了与其它离子产生化学反应的带电离子的电位。
摩尔浓度是另一种通过分子数量来表示浓度的方法,但并不考虑电位。当溶质溶於溶剂中,其摩尔量等於分解在每升溶液中分子摩尔浓度,摩尔浓度等於重量浓度除以分子重量。
在稳定的溶液中,我们用CaCO3来表示其正离子与负离子的总数必须相等。与水分析的精度有关,碳酸钙中的阳离子总数几乎等於阴离子的总数。一种精确分析将会给出总的阴离子的浓度是在总的阳离子浓度的10%范围之内。
许多实验室没有直接测试水中的钠离子浓度的能力,它们会通过阴离子的总浓度中减去阳离子浓度来得出钠离子的浓度(都表示为碳酸钙)。一些实验室会用这种方法来得出硷性溶液去保证电荷平衡,这些方法是加阳离子和阴离子(如用碳酸钙),如它们的总数是相等,实验室用数学方法得出钠或硷溶液的浓度是可能的。如果其总数大於10%,则其分析方法的精度不够理想。
(六)pH:
测量pH值是水分析中十分重要的一项。pH值会极大地影响弱可溶性盐的溶解性。水的pH值即表示它的酸硷性,在水中(H2O),一定量的分子会自然游出阳离子(即氢离子)和其阴离子(即氢氧根离子)。在华氏77度(摄氏25度)下,离子的浓度是一个粗略的常数,其值为0.00000000000001,10的-14次方或10-14
[H+]x[OH-]=10-14
公式中用[ ]括起来的通常表示某一离子的浓度。
如果在水中加入酸或硷,氢或氢氧离子会结合成水以维持同样的氢和氢氧离子的浓度常数。举例来说,如果酸(会释放出氢离子的化学剂)被加入水中,氢离子将会与一些氢氧离子结合形成水,因此降低了氢氧离子的浓度,也就是维持其值在10-14。
pH值是由摩尔浓度中氢离子的负对数(以10为底)来表示的(摩尔/升),在数学上,pH值由以下两个公式所定义:
[H+]=10-pH
pH= - log[H-]
举例来说:
如果氢离子浓度为0.01mg/L时,水的pH值是多少?
答案:
氢的分子重量为每摩尔1克,即等於1.000g/ml。
(0.01mg/L)÷(1000mg/mole)=0.0001moles/L
0.0001moles/L=10-5moles/L
pH=-log(10-5moles/L);pH=5
举例来说:
溶液浓度为100mg/L的硫酸的pH值为多少?
答案:
硫酸(H2SO4)的分子重量是由其分子的组成元件的分子重量所决定的:
2个氢1x2=2克/摩尔
1个硫32x1=32克/摩尔
4个氧16x4=64克/摩尔
100毫克÷98.000毫克/摩尔=0.001摩尔/升硫酸
硫酸是强酸,这意味着它会在水中完全分解。这种分解会释放出两个氢离子,因此,其氢离子的摩尔浓度(摩尔/升)等於硫酸根离子的摩尔浓度的两倍。
pH= -log[0.001摩尔/升 x 2]=2.7
在这个例子中,水中原始的氢离子的浓度为10-7(0.0000001)摩尔/升是忽略不计的。当氢离子浓缩与硫酸根离子相比(0.02摩尔/升)是可以忽略不计的。
(七)硬度:
钙和镁是产生水硬度的主要因素,从技术上来说,考虑水的硬度还要考虑其他因素,尽管与钙和镁相比其他浓度可以忽视不算。
硬度和硬水的来由是因为多价阳离子如钙和镁会吸附天然皮肤油脂,它会使皮肤感到很"硬"。
硬度的正电荷特性会使它被磷酸盐(一种极强的酸)结合在一起,大多数清洁剂采用磷酸盐或一些其它的阳性表面活化剂,硬度会降低清洁剂去除污垢的能力,当清洁剂加入硬水中,水中的泡沫明显减少。
硬度对RO系统是非常重要的,因为高浓度重碳酸盐、碳酸盐、硫酸盐、氟化物和矽酸盐是不溶的。大多数天然水源中都存在硬度,要获得RO系统最佳的使用性能,控制钙和镁的沉淀是非常必要的。
(八):
钠盐在水中的溶解性极强,水软化剂就是用树脂交换水中的钠,当树脂接近钠时,会产生氯化钠,用钠去替换先前已除去的硬度阳离子。
钠在某些超纯水应用中应加以注意,因为钠是单价的离子(包含一个正的单价电荷),它不像另外的离子一样能被RO膜所隔离出来,它也不能被下段离子交换设备所提取。因此,超纯水系统在半导体生产制造中,水中存在的微量钠离子会导致整个集体电路的失效。
(九):
硷性可除去溶液中的氢离子,这些阴离子包括重碳酸,碳酸和氢氧基。它们能去除氢离子,因此能转换氢和氢氧离子的比率,它能提高水的pH值(大於正常的pH值)。
在大多数天然水源中,不是全部的硷性都是以碳酸(HCO3)存在的。碳酸盐的硷性通常是作为滴定法测量浓度化学剂,硷性是用甲基橙色来显示的。pH值低於8.3时,大多数的硷性会被一定浓度的可溶性二氧化碳所平衡。
当水源的pH值大於8.3时,大多数硷度是以酸根的形存在。硷度在大多数水源作为天然pH值的缓冲剂,在自然界是通过各种硷度形成和可溶二氧化碳之间的转换去抵制能引起污染的pH值的变化。
假如水能溶解大气中的二氧化碳形成碳酸,酸性水流经或流入地表时会溶解碳酸钙,这种溶解会不停的发生直到水中的pH值增加,然後便不会侵蚀碳酸钙。
在水中的重碳酸盐过饱和而水仍是酸性,过量的重碳酸盐将会转变成二氧化碳,水中的二氧化碳过饱和,过量的二氧化碳会变作气体进入大气中。
水中的碳酸盐过饱和而水是硷性的,过量的重碳酸盐阴离子将会转换成碳酸阴离子。假如因为一些原因使水中的碳酸盐在非常硷性的pH值下过饱和,过量的碳酸盐将离开溶液,任何多余的硷性会直接以氢氧离子的形式存在。
因为水能吸收硷度,所以大多数天然水源中的碳酸钙接近於饱和状态。如果水在RO系统中被浓缩,碳酸钙盐通常会被沉淀出来,这种状况发生得极快,并且领先於其它任何一种盐形成,从某种意义上来说大多数的RO系统都要防止和控制碳酸钙的沉淀。
(十):
硫酸盐在许多天然水中浓度相对较高。当我们需要控制pH值时常把硫酸盐以酸的形式加入水中。在RO系统中通过减少或控制天然水中的二价阳离子以防止硫酸盐水垢的形成。
(十一):
氯化物在水垢形成这一点上对RO系统的威胁较小。几乎所有的氯化盐在水中都是可溶的。
在RO系统中高浓度的氯化盐能侵略SUS304。假如氯在RO系统中超出几千个ppm,在高压管道中需要用316L不锈钢以防止腐蚀。
(十二):
氟化物浓度在许多水源中通常较低。假如氟化物恰巧存在可知浓度的溶液中,氟化钙也是不溶的。
(十三)硝酸盐:
硝酸盐的溶解性不是我们所关注的。如果水中存在硝酸盐,我们更加关注的是水处理系统能除去它们的能力。当饮用水中的硝酸盐被哺孔动物(包括人类)所吸收时会产生亚硝酸盐。这些亚硝酸盐会妨碍人类血液交换氧气的能力,它会对胎儿以及儿童或其它哺乳动物产生一系列问题,因为这个原因,我们希望控制饮用水中的硝酸盐的浓度低於40毫克/升。
因为硝酸盐的弱电荷特性不易被RO系统所除去,也不易被阴离子交换树脂去除。根据膜和系统的回收量,硝酸盐可被RO系统去除的范围在50%到90%之间。
(十四)铁和锰:
是以还原状态的形式在水中被发现,它是可溶性的,又以氧化状态的形式存在於水中,它是不溶性。氟化物浓度在许多水源中通常较低。假如氟化物恰巧存在可知浓度的溶液中,氟化钙也是不溶的。大多数铁通常以两种金属形式存在於天然水源中,二价铁状态(Fe2+)是可溶性的,被氧化後的三价铁状态(Fe3+)是不溶性的,并能污染RO系统。
在井水铁的含量是主要的,最明显的是泵开始生锈。假如用黑铁或碳钢做管道系统、容器或容器接头则预处理设备就会产生铁。假如有酸注入设备的上游,这个问题会进一步复杂化。
如果在RO膜进给水中铁和锰的浓度大於0.05毫克/升,就需要考虑去除它们,如果铁和锰处理还原(溶解)状态,它可不会对RO系统引起任何污染问题。如果空气进入系统或入某些氧化剂,铁和锰就会被氧化成不溶状态,它又会进一步污染膜元件。它也能对剩余的氧化剂起催化作用,可能也会损坏或降低RO膜的性能。
(十五)钡和锶:
在天然水中一般不包括钡和锶溶液。如果有相对浓度极小的(0.01毫克/升或更多)钡和锶与硫酸盐在一起,它们极易被析出膜表面而形成水垢。去除硫酸钡和硫酸锶水垢是极不容易的,因此,防止盐的沉淀是非常重要的。
(十六)铝:
铝一般不存在在天然水源中,因为是三价的铝,所以有很高的电荷特性,其相对尺寸较小(分子重量为27)。它会导致铝金属离子有高的的电荷密度,这使得铝十分活跃。
铝与铁在许多方面相似,它会起反应。与铁相同,铝会与氧结合形成不溶性的氧化物。这两种金属都会与负电荷的有机胶体相混合,当矽酸存在时会沉淀出来。
因为铝的高电荷特性。许市政用铝盐[硫酸铝Al2(SO)4或偏铝酸钠[NaAlO2]附加剂加入地表水的处理系统中。铝能凝结水中不溶性的带负电荷有机悬浮固体的作用。这使悬浮固体集结在一起析出悬浮溶液中。
当水的pH值很小或很大时铝变得十分易溶,当RO的pH值范在5.3到8.0时就较难溶於水。因此,如果市政水处理工厂既用铝又用偏铝酸钠作添加剂时,RO膜又注入酸时铝的污染必须加以重视。在这种情况下,酸的注入必须放在介意过滤器的上流部分,微量铝在渗析工业中被极为关注。当渗析用水中铝的浓度大於0.01毫克/升应对肾渗析病人的健康有害。
(十七)铜和锌:
在天然水源中基本不存在的铜和锌,然而,管道材料中获得一些微量浓度也是有可能的。
随着pH值的增加,铜和锌被析出溶液,在RO系统中就像盐被析出一样。因为在进给水中正常的pH值下铜和锌的浓度通常较低。当这些沉淀留在水中过长时间会影响RO系统的性能。
分析铜和锌在RO进给水中的主要原因是由於要考虑使用聚合物膜,作为过滤元素,铜和锌会增强氧化剂氧化性能,在用聚合膜时,特别是当强酸或过氧化氢被用於消毒时,这些必须加以重视。
(十八)矽盐:
是一种对RO系统特别有趣和危险的离子,因为它析出溶液後会变的很稳定,pH值在9以下时,矽在大多数情况下以矽酸的形式存在(H4SiO4也写作Si(OH)4,在pH值较低时,矽酸会聚合成胶状物(通常我们称之为矽胶)。当水的pH值超过8时,矽酸分解出矽酸离子(SiO3-2),在高的pH值时,它会与钙、锰、铁或铝相结合沉淀出盐。
矽和矽酸盐是不再溶的,双氟化铵溶液能去除不严重的矽垢,但是,双氟化铵认为是一种较危险的化学物质,处理它是比较困难的。
矽的可溶生是由温度和pH值所决定的。如果在RO进给水中矽的浓度大於20毫克/升时,就应考虑除去矽的沉淀物。
(十九)硫化氢:
在佛罗里达的浅井水中经常会发现硫化氢(H2S),硫化氢是一种可溶性气体。会被大气中的氧所氧化,或在生物控制中通过把氯加入水中而变成硫磺沉入水中。RO系统的进给水中存在H2S时也能运行良好,只是由於系统接触空气,有时会有硫磺污染问题。
只要将水经过除味器就能去除硫化氢气体,硫化氢气体能散发出臭鸡蛋气味。除味器能除去硫化氢气体,因此在一些地方不准使用。
另外一种去除硫化物的方法是故意通过注氯或另外方法去氧化它们。介质过滤器被用於去除沉淀的硫磺。
(二十)磷酸盐:
是负三价的,有极强的负电荷特性,能与多价的阳离子相互作用。在正常的pH值下磷酸钙溶解性极弱,在高的pH值下磷酸钙溶解性极弱,在高pH值下可溶性更低。
如果磷酸盐以任何可知的形态存在於RO进给水系统中,除非水是酸性的,磷酸盐会沉入溶液落入RO系统中。它是通过当纯净水渗透入膜时增加了磷酸盐的浓度和当水的浓度增加时RO系统中的pH值提高所引起的。
沃特浦全国免费咨询热线:400-626-4939
欢迎广大客户来电垂询,沃特浦竭诚为您服务
下一篇:工业用水铁、锰处理技术









